Nombres vernáculos
Distribución geográfica
Trópicos y zonas templadas del mundo.
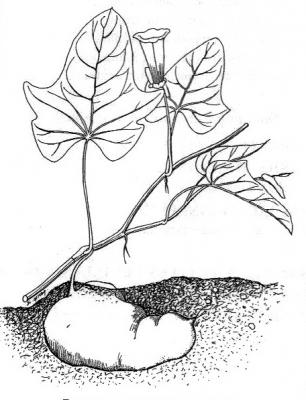
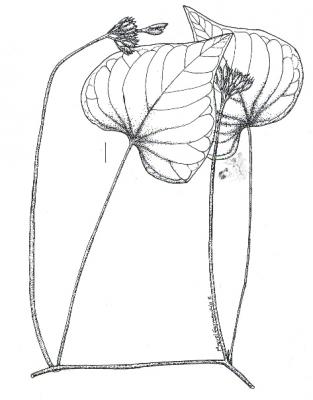
Descripción botánica
Enredadera perenne con raíz tuberosa comestible. Tallo, algo suculento pero algunas veces delgado y herbáceo, glabro o pubescente, ramificado. Hojas de cordadas a ovadas, enteras, dentadas o profundamente lobadas, de 5 a 10 cm de largo, glabras o raramente pubescentes, ápice agudo a acuminado, mucronado. Inflorescencias cimosas a cimoso-umbeladas con pocas flores; flores con sépalos oblongos; corola campanulada con limbo color lavanda a púrpura-lavanda y garganta más oscura, blanca en algunas variedades. Cápsula ovoide, glabra, café clara a pajiza, bilocular, 4-valvada; semillas 4, glabras café obscuras a café.
Voucher(s)
Jiménez,131,JBSD
Farmacopea
Ed.3References
1 GERMOSÉN-ROBINEAU L, GERÓNIMO M, AMPARO C, 1984
Encuesta TRAMIL. enda-caribe, Santo Domingo, Rep. Dominicana.
2 NAKATANI M, KOMEICHI M, 1991
Distribution of endogenous zeatin riboside and abscisic acid in tuberous roots of sweet potato. Nippon Sakumotsu Gakkai Kiji 60(2):322-323.
3 NAKATANI M, KOMEICHI M, 1991
Chantes in the endogenous level of zeatin riboside, abscisic acid and indole acetic acid during formation and thickening of tuberous roots in sweet potato. Nippon Sakumotsu Gakkai Kiji 60(1):91-100.
4 BURKA L, FELICE L, JACKSON S, 1981
6-oxodendrolasin, 6-hydroxydendrolasin, 9-oxofarnesol and 9-hedroxyfarnesol, stress metabolites of the sweet potato. Phytochemistry 20:647-652.
5 WOOD G, HUANG A, 1975
The detection and quantitative determination of ipomeamarone in damaged sweet potatoes (Ipomoea batatas). J Agr Food Chem 23(2):239-241.
6 BURKA L, KUHNERT L, 1977
Biosynthesis of furanosesquiterpenoid stress metabolites in sweet potatoes (Ipomoea batatas) oxidation of ipomeamarone to 4-hydroxymyoporone. Phytochemistry 16(12):2022-2023.
7 BURKA L, KUHNERT L, WILSON B, HARRIS T, 1974
4-hydroxymyoporone, a key intermediate in the biosynthesis of pulmonary toxins produced by Fusarium solani infected sweet potatoes. Tetrahedron Lett 15(46):4017-4020.
8 MINAMIKAWA T, AKAZAWA T, URITANI I, 1962
Isolation of esculetin from sweet potato roots with black rot. Nature(London) 195:726-727.
9 SONDHEIMER E, 1958
On the distribution of caffeic acid and the chlorogenic acid isomers in plants. Arch Biochem Biophy 74(1):131-138.
10 MIYAZAKI T, TSUZUKI W, SUZUKI T, 1991
Composition and structure of anthocyanins in the periderm and flesh of sweet potatoes. Engei Gakkai Zasshi 60(1):217-224.
11 OSAGIE AU, 1977
Phytosterols in some tropical tubers. J Agr Food Chem 25(5):1222-1223.
12 MATLACK MB, 1935
A phytosterol and phytosterolin from the sweet potato. Science 81:536.
13 DE ALMEIDA LB, PENTEADO M, BRITTON G, UEBELHART P, ACEMOGLU M, EUGSTER C, 1988
Isolation and absolute configuration of beta, beta-carotene diepoxide. Helv Chim Acta 71(1):31-32.
14 DE ALMEIDA LB, PENTEADO M, SIMPSON K, BRITTON G, ACEMOGLU M, EUGSTER C, 1986
Isolation and characterisation of (5R,6S,5'R,8'R)-and (5R,6S,5'R,8'S)-luteochrome from Brazilian sweet potatoes (Ipomoea batatas Lam.). Helv Chim Acta 69(7):1554-1558.
15 HASHIZUME T, SUYE S, SOEDA T, SUGIYAMA T, 1982
Isolation and characterization of a new glucopyranosyl derivative of 6-(3-methyl-2-butenylamino) purine from sweet potato tubers. Febs Lett 144(1):25-28.
16 HASHIZUME T, SUYE S, SUGIYAMA T, 1981
Occurrence and level of cis-zeatin riboside in sweet potato tubers (Ipomoea batatas L). Nucleic Acids Symp Ser 10:131-134.
17 OHTA T, OMORI T, SHIMOJO H, HASHIMOTO K, SAMUTA T, OHBA T, 1991
Identification of monoterpene alcohol beta-glucosides in sweet potatoes and purification of a shiro-koji beta-glucosidase. Agr Biol Chem 55(7):1811-1816.
18 KOLATTUKUDY P, KRONMAN K, POULOSE A, 1975
Determination of structure and composition of suberin from the roots of carrot, parsnip, rutabaga, turnip, red beet and sweet potato by combined gas-liquid chromatography and mass spectr. Plant Physiol 55(3):567-573.
19 DOWNTON WJ, HAWKER JS, 1975
Evidence for lipid-enzyme interaction in starch synthesis in chilling-sensitive plants. Phytochemistry 14:1259-1263.
20 LE GRAND A, 1985
Les phytothérapies anti-infectieuses (partie 3: Une Evaluation) Amsterdam, Pays-Bas.
21 WALKER BS, JANNEY JC, 1930
Estrogenic substances. II. An analysis of plant sources. Endocrinology 14(6):389-392.
22 MIWA M, KONG Z, SHINOHARA K, WATANABE M, 1990
Macropohage stimulating activity of foods. Agr Biol Chem 54(7):1863-1866.
23 TANAKA Y, KATAOKA M, KONISHI Y, NISHMUNE T, TAKAGAKI Y, 1992
Effects of vegetable foods on beta-hexosaminidase release from rat basophilic leukemia cells (RBL-2H3). Jpn J Toxicol Environ Health 38(5):418-424.
24 VANDANA PANDA V, SONKAMBLE M, PATIL S, 2011
Wound healing activity of Ipomoea batatas tubers (sweet potato). Functional Foods in Health and Disease 10:403-415.
25 AGUILAR CONTRERAS A, ZOLLA C, 1982
Plantas Tóxicas de México. División de información etnobotánica. Ciudad, México: Unidad de investigación biomédica en medicina tradicional y herbolaria del Instituto Mexicano del seguro social. p118-120.
26 ORTALIZA IC, DEL ROSARIO IF, CAEDO MM, ALCARAZ AP, 1969
The availability of carotene in some Philippine vegetables. Philippine J Sci 98(2):123-131.